
Přemýšlíte při nákupu zeleniny, ovoce, rohlíků nebo třeba vína nad tím, jaké látky byly použity pro jejich vypěstování nebo vyprodukování a jak na vás i životní prostředí působí? Tým doc. RNDr. PhDr. Ing. Jany Jaklové Dytrtové, Ph.D., který propojil výzkumníky z Ústavu organické chemie a biochemie AV ČR, University of Helsinki, Univerzity Karlovy a České zemědělské univerzity v Praze, si takové otázky kladl. Podařilo se mu díky tomu získat nové informace o přeměnách a účincích běžně využívaných pesticidů – triazolů při pěstování plodin, jejichž účinek je silně ovlivněn jejich reaktivitou s ostatními složkami životního prostředí, především biologicky aktivních látek (zejména enzymů, antioxidantů a biogenních prvků).
Triazoly jsou chemicky poměrně homogenní skupinou látek, které mají široké uplatnění především v ochraně rostlin před houbovými škůdci, jako antimykotika v medicíně či k léčbě postmenopausální rakoviny prsu. Triazoly reagují i s dalšími biologicky aktivními látkami, čímž mění jak své vlastnosti, tak vlastnosti látek, se kterými interagují a zásadním způsobem ovlivňují biologickou rovnováhu v organismech i životním prostředí.
Triazoly byly speciálně vyvinuty, aby blokovaly enzym 14α-demethylázu, který je klíčový pro biosyntézu ergosterolu u hub a bakterií. Tímto biochemickým způsobem je poměrně efektivně blokován růst houbových patogenů, kterým se nedostává ergosterolu jako funkční součásti jejich membrán. Na druhou stranu tato biochemická inhibice houbových patogenů není příliš selektivní. Je to díky podobnosti enzymu 14α-demethylázy napříč rostlinnou, živočišnou, bakteriální i houbovou říší. Velkým potenciálem triazolů je tedy blokovat 14α-demethylázu i v necílových organismech. Dalším enzymem, který je takto utlumován, je aromatáza. Tento enzym souvisí například s rovnováhou mezi ženskými a mužskými pohlavními hormony. Tímto se triazoly řadí mezi významné endokrinní disruptory a ukazuje se, že je třeba jejich účinky na necílové organismy včetně člověka studovat v kontextu přítomnosti dalších interagujících složek.
V tomto projektu jsme se zaměřili na koktejlové interakce triazolových fungicidů a jejich vliv na vybrané enzymy. Především bylo cílem popsat vliv triazolů (penkonazolu, cyprokonazolu a tebukonazolu) na aktivitu enzymu aromatázy v přítomnosti kationtů stopových prvků (mědi a zinku), popsat, které komplexy vznikají v přítomnosti kationtů stopových prvků, jak ovlivní triazoly v přítomnosti stopových prvků chování významných antioxidantů (resveratrol) a jakým způsobem aplikace triazolů v reálných podmínkách ovlivní produkci fenolických látek v plodech rajčat, obsah chlorofylu v zelených částech rostliny rajčete jedlého a další růstové parametry této rostliny. V neposlední řadě bylo cílem vyvinout vhodné analytické metody pro stanovení triazolů v plodech rajčat.
Bio nebio jedno rajče aneb Vliv aplikace triazolů na růst rajčete jedlého i obsah fenolických látek a triazolů v jeho plodech
Rajčata byla pěstována v nádobách za definovaných podmínek a ošetřována různou kombinací běžně používaných triazolů (penkonazol, cyprokonazol a tebukonazol – aplikovány jednotlivě nebo v kombinaci po dvou či po třech) proti houbovým onemocněním v pravidelném intervalu, každých 14 dní.
Rostliny rajčat ošetřovaných triazoly byly oproti rostlinám neošetřovaným celkově menší, dříve plodily a plody byly větší. Zvláště patrný byl snížený nárůst zelené biomasy, který se projevil zejména u listů a tenkých stonků, tedy ve fotosynteticky nejvíce aktivních pletivech. Tento efekt byl nejsilnější u rostlin ošetřovaných penkonazolem, nebo směsí penkonazol obsahující (nejvíce u směsi penkonazolu a tebukonazolu). Ošetřování triazoly též změnilo obsah flavonoidů, zejména u látek, u kterých se předpokládají antioxidační účinky (například kvercetin nebo hesperidin) došlo ke zvýšení obsahu flavanoidů. Na druhou stranu, z předchozích experimentů (viz dále) víme, že triazoly mají schopnost interagovat zejména s ionty Cu2+, kdy dochází k produkci Cu+, které jsou často iniciačním místem pro produkci volných radikálů (takzvaná Fentonova reakce). Je tedy pravděpodobné, že přítomnost triazolů změnila antioxidační podmínky a rostliny na to reagovaly zvýšenou produkcí některých flavonoidů s antioxidačními účinky. Zvýšenou produkcí plodů rajčat (včetně zvětšení velikosti plodů) rostlina zřejmě v důsledku zhoršených růstových podmínek investovala do zajištění svého potomstva (semen).
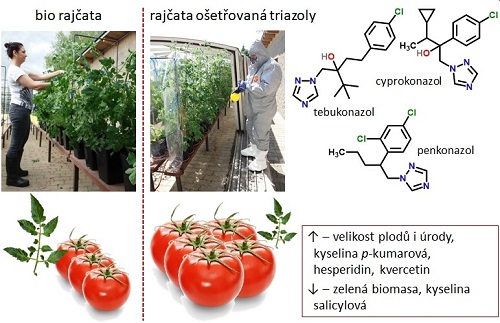
Obr. 1 Zelená biomasa rajčete jedlého ošetřovaného triazoly byla menší (až o polovinu) v porovnání s „biorajčaty“. Na druhou stranu plody triazoly ošetřovaných rajčat byly výrazně větší (až o 30%) v porovnání s neošetřenými. Ošetření triazoly též měnilo obsah některých flavonoidů.
Když si namícháte koktejl z triazolů a mědi (zinku)… aneb Vliv koktejlu triazolů a iontů mědi na aktivitu enzymu aromatázy
V zemědělské praxi se ukazuje, že je k ochraně výhodnější aplikovat triazoly ve směsi několika různých triazolů. Nabízí se zde otázka, zda se bude měnit efekt těchto triazolových směsí v porovnání s čistými látkami (při zachování stejné celkové koncentrace triazolů). Navíc, jakmile se triazoly dostanou do reálného prostředí (obsahující různé potenciálně interagující látky), nebude se zde významně měnit jejich reaktivita i vliv na klíčové enzymy – zejména aromatázu (enzym, který katalyzuje přeměnu mužských pohlavních hormonů na ženské)?
Studiem se především ukázalo, že jednotlivé triazoly neinhibují enzym aromatázu stejně – nejvíce ji inhiboval penkonazol (aktivita na 44 %), následovaný cyprokonazolem a tebukonazolem (72 a 77 %). Různé kombinace těchto tří triazolů (při zachování stejné celkové koncentrace triazolů, 10-6 mol/L) nevykazovaly větší ani menší inhibiční efekt na aromatázu oproti teoretickému odhadu. Na druhou stranu, přítomnost Cu2+ výsledný efekt triazolů zásadním způsobem měnila. Nejvíce se inhibiční efekt prohloubil u kombinace penkonazol + Cu2+, či u kombinací penkonazol obsahujících (penkonazol + tebukonazol + Cu2+, penkonazol + cyprokonazol + Cu2+ nebo penkonazol + tebukonazol + cyprokonazol + Cu2+), kdy se inhibiční efekt zvýšil o 40% oproti teoretickému odhadu. Hlavním důvodem tohoto chování jsou především přeměny penkonazolu v přítomnosti Cu2+. V systému penkonazol a Cu2+ totiž dochází k přeměnám penkonazolu (ztráta jednoho Cl, vznik komplexů s ionty mědi, dehydrogenace vedoucí ke vzniku dalšího kruhu ve struktuře a k redukci Cu2+ na Cu+). Zejména vznik Cu+ může být potenciálně nebezpečný, a to nejen pro samotnou aktivitu aromatázy, ale také pro možnost iniciace takzvané Fentonovy reakce vedoucí k produkci volných radikálů, které tak často předcházejí samotnému poškození buněčných struktur.
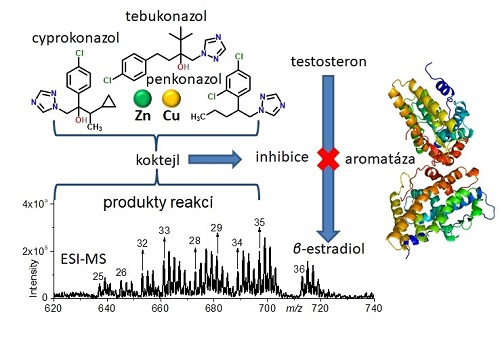 Obr. 2 Čím je koktejl interagujících látek složitější, tím více produktů reakce může vzniknout. Nicméně výslednou aktivitu enzymu aromatázy je možné určit na základě aktivity NADPH (nikotinamidadenindinukleotidfosfát, kofaktor oxidačně-redukčních dějů v buňce) a jednotlivé produkty reakce zase pomocí ESI-MS (hmotnostní spektrometrie s ionizací elektrosprejem).
Obr. 2 Čím je koktejl interagujících látek složitější, tím více produktů reakce může vzniknout. Nicméně výslednou aktivitu enzymu aromatázy je možné určit na základě aktivity NADPH (nikotinamidadenindinukleotidfosfát, kofaktor oxidačně-redukčních dějů v buňce) a jednotlivé produkty reakce zase pomocí ESI-MS (hmotnostní spektrometrie s ionizací elektrosprejem).
Je libo sklenku vína? Aneb antioxidanty ve víně v širším kontextu.
Kdo by si rád nezpříjemnil pěkný večer s přáteli sklenkou dobrého vína? Ta se dá dokonce ospravedlnit vědecky podloženými fakty, že trocha alkoholu působí pozitivně na náš kardiovaskulární systém a také tím, že víno obsahuje antioxidanty, které působí proti stárnutí. Tak jako to není jednoduché s pitím alkoholu (ukazuje se, že pozitivně působí jen ve velmi malých množstvích, a to pouze na srdce a cévy), tak to jednoduché není ani s opěvovanými a propagovanými antioxidanty.
Asi nejznámějším antioxidantem přítomným ve víně (zejména červeném) je resveratrol. S resveratrolem je ale potíž; je sice velmi dobře rozpustný v alkoholu, ale téměř nerozpustný ve vodě. Z toho vyplývá, že se ho jen velmi málo dostane krevním řečištěm do buněk. Jako všechny antioxidanty, tak i resveratrol je vysoce reaktivní. Otázkou tedy je, na co se může přeměnit v samotném víně (kde je na rozdíl od krve celkem slušně rozpustný). Možností je celá řada, proto se omezíme především na měďnatý kation (v minulosti se totiž vinice proti plísňovým onemocněním ošetřovaly zejména roztokem modré skalice – síranu měďnatého a viniční půda je tak na mnoha místech mědí v podstatě kontaminována). Výsledek vzájemné interakce měďnatého kationtu a resveratrolu nás opravdu nepotěší. Resveratrol totiž v přítomnosti Cu2+ ztrácí své antioxidační účinky a Cu2+ se redukuje na Cu+, která opět iniciuje Fentonovu reakci (tedy produkci volných radikálů). Resveratrol v kombinaci s měďnatými kationty tedy působí zcela opačně, než bychom očekávali – tedy pro-oxidačně! A jak celou situaci promění přítomnost triazolu? V tomto případě tebukonazolu (fungicidu používaného ve vinici dnes)? Navzdory možným očekáváním, tebukonazol v této směsi nebo koktejlu působí pozitivně. Tvoří totiž s kationty mědi velmi stabilní komplexy, čímž je znepřístupňuje pro reakce s resveratrolem, nebo pro následnou iniciaci Fentonovy reakce.
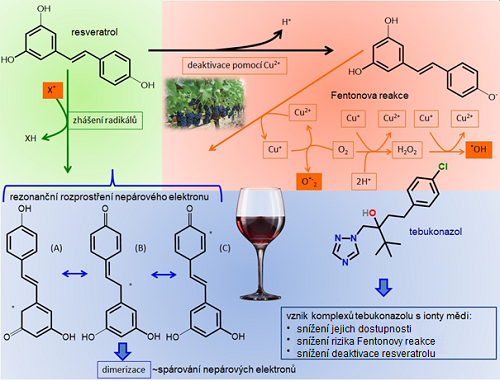
Obr. 3 Popis působení resveratrolu. Zeleně: antioxidační účinky v podobě zhášení volných radikálů, oranžově: deaktivace resveratrolu působením Cu2+ a Fentonova reakce, modře vlevo: vznik dimerů resveratrolu ze dvou radikálů resveratrolu, modře vpravo: tvorba komplexů iontů mědi s tebukonazolem = snížení dostupnosti iontů mědi
Nic není černobílé
I látka, která na náš organismus, či životní prostředí primárně nepůsobí pozitivně, může sehrát pozitivní roli. Na druhou stranu, bez triazolů a dalších fungicidů (pesticidů) bychom jen těžko vypěstovali dostatek plodin pro nasycení stále narůstající lidské populace. Studovat reakce vícesložkových směsí, to jest koktejlů, není snadné (je k tomu potřeba kombinace několika experimentálních instrumentálních i výpočetních metod), ale výsledky těchto studií nám pomohou se správnou aplikací, či rozhodováním o podmínkách a optimalizaci použití těchto látek.
Autorství: Ústav organické chemie a biochemie AV ČR