
Makromolekulární chemik Peter Košovan z Přírodovědecké fakulty Univerzity Karlovy propojuje teoretické modely, počítačové simulace a laboratorní experimenty. Zkoumá, jak se náboj velkých molekul mění v závislosti na pH a jak tyto změny ovlivňují jejich chování.
Peter Košovan se svými kolegy studuje principy, podle kterých fungují interakce mezi nabitými makromolekulami (velkými molekulami). Zaměřuje se především na případy, kdy jsou experimentálně pozorované interakce ve zdánlivém rozporu s chemickou intuicí a obecně známými pravidly. Například proč některé experimenty naznačují přitažlivé interakce mezi stejně nabitými molekulami, které by se měly přirozeně odpuzovat. „Už během magisterského studia jsem se chtěl věnovat teorii, simulacím a experimentům současně. To se ukázalo jako úkol vysoko nad možnosti jednoho studenta, proto trvalo dalších zhruba 15 let, než se mi to povedlo úspěšně realizovat,“ popisuje výzkumník.
Zajímá ho, jakým způsobem se při interakci mezi molekulami mění jejich náboj tak, aby tato interakce byla energeticky výhodná, a jak toho lze dosáhnout pomocí změny pH v roztoku. Při interpretaci většiny chemických experimentů se obvykle vychází z předpokladu, že náboj molekul se při jejich vzájemné interakci nemění. „Naše teoretické modely i experimenty však ukazují, že v mnoha případech je tomu jinak. Nejenže náboj molekul určuje jejich vzájemné interakce, ale funguje to i obráceně: interakce mezi molekulami také ovlivňují jejich náboj,” vysvětluje Košovan.
Makroskopicky se změna mezimolekulových interakcí projeví například vysrážením z roztoku, změnou skupenství nebo rozdělením na různé fáze.
Biomolekuly jsou také makromolekuly
Výsledky výzkumu Petera Košovana ukazují, že modely, které používá pro vysvětlení chování syntetických polymerů, lze použít také na vysvětlení chování biomakromolekul – peptidů a proteinů. „Je vždy velmi zajímavé pozorovat jev předpovídaný na základě jednoduchého teoretického modelu také v reálném experimentu. Ještě zajímavější je, když za mnou přijdou kolegové se zdánlivě nečekaným experimentálním pozorováním a já jim mohu říci, že už mám jednoduchý model, který to vysvětluje,“ říká o výzkumu, na němž spolupracoval s kolegy z německého Stuttgartu, Nizozemska, Rakouska, Norska a dalších zemí.
Vše začalo v roce 2018, kdy za Petrem Košovanem přišli kolegové z Nizozemska s dotazem, zda by dokázal vysvětlit, jakým mechanismem se různě nabité proteiny akumulují uvnitř tzv. polyelektrolytových koacervátů. Ty se připravují smícháním dvou opačně nabitých polymerů, přičemž vzniknou dvě kapalné fáze – jedna obsahuje polymery, druhá převážně vodu. Nizozemští kolegové vypozorovali, že v případě dvou téměř identických proteinů, které se liší jen nábojem několika málo skupin, se jeden z nich hromadí v polymerní a druhý ve vodní fázi. Po změně pH si oba proteiny vymění role. „Věděl jsem, že proteiny modelovat neumíme, ale měl jsem nadaného studenta, a tak jsem se rozhodl vzít to jako výzvu. Student Roman Staňo tehdy výzvu přijal a stala se tématem jeho diplomové práce, za kterou později dostal cenu od firmy Contipro.“

Vlevo: molekulární model pro simulace fázové rovnováhy mezi polyelektrolytovým koacervátem (PEC) a supernatantem (roztokem, který obsahuje pouze malé ionty); Vpravo: fotografie skutečného koacervátu v rovnováze se supernatantem, jehož chování jsme studovali pomocí simulací i experimentů. (Obrázky z publikace, Autor: Dr. Roman Staňo)
Výzkumníci během pěti let vytvořili model, který vysvětlil jevy pozorované v experimentu, a navrhli nové experimenty potvrzující předpovědi modelu. Tento příklad ukázal, že jednoduché modely běžně používané pro syntetické polymery složené ze stejných opakujících se jednotek mohou vysvětlit i chování proteinů, jejichž vlastnosti jsou určeny složitou sekvencí různých aminokyselin.
„Úspěch s pochopením chování proteinů nás motivoval a začali jsme zkoušet, jak daleko lze s jednoduchými modely zajít. Oslovili jsme kolegy ze skupiny Soft Matter, zakoupili speciální peptidové sekvence a začali zkoumat, jak spolehlivě naše modely dokážou předpovědět náboj těchto peptidů při různém pH,” popisuje vědec. Ukázalo se, že modely předpovídají náboj peptidů velmi dobře. Často se od experimentů odchylují méně, než činí neurčitost samotného experimentu. To se později potvrdilo pro řadu různých vzorků peptidů i syntetických polymerů.
Od kapek v buňce k modelům pro medicínu
Přibližně ve stejné době, kdy se tým Petra Košovana začal zabývat proteiny v syntetických koacervátech, se ukázalo, že podobná fázová separace probíhá i v živých buňkách: vznikají zde kapičky s vysokou koncentrací proteinů – bezmembránové organely (biomolekulární kondenzáty). Ty lokálně zvyšují koncentraci vybraných molekul, posouvají termodynamickou rovnováhu a umožňují tak reakce, které by mimo kondenzát neprobíhaly, což připomíná chování koacervátů.
Vznik kondenzátů navíc dobře popisují klasické modely fázové separace polymerů z 50. let, protože v kondenzátech často dominují nestrukturované, flexibilní a mnohdy silně nabité proteiny blížící se polymerům. V poslední dekádě se proto rozvíjí směr, který tyto zavedené teorie využívá k předpovědi různých jevů v kondenzátech – mimo jiné vlivu pH, kde důležitou, ale těžko měřitelnou veličinu představuje rozdíl mezi pH uvnitř kondenzátu a vně.
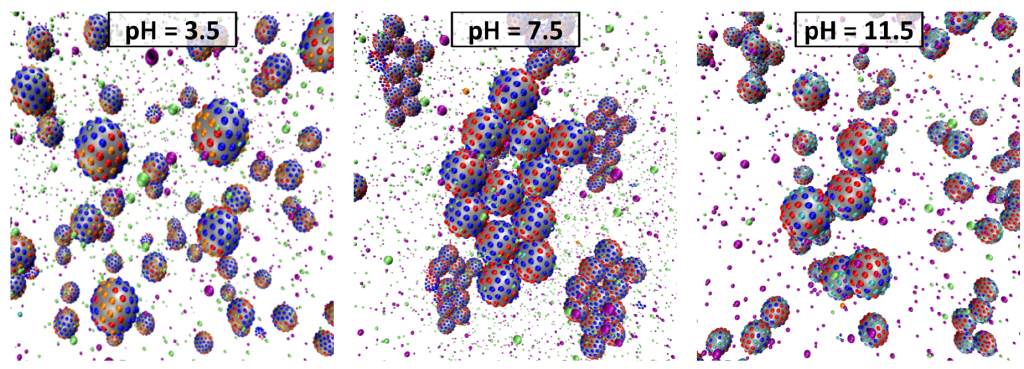
Koloidní nanočástice jako zjednodušený model pro interakce globulárních proteinů v roztocích při různém pH. Červené a modré tečky představují kyselé a bazické skupiny, jejichž náboj se mění v závislosti na pH. Změna náboje ovlivňuje tendenci částic k agregaci, která vede k jejich vysrážení z roztoku. (Nepublikováno, Autor: Dr. Sebastian Pineda Pineda; video)
Na tuto mezeru cílí Košovanovy nové projekty: modely ověřené na syntetických polymerech a peptidech by mohly pomoci predikovat pH a chování biomolekulárních kondenzátů i koncentrovaných roztoků globulárních proteinů, například terapeutických monoklonálních protilátek zahušťovaných až na hranici rozpustnosti. V membránových separacích je volba pH zásadní a kvůli Donnanově rovnováze se pH na straně proteinového roztoku může lišit od pufru. Protilátky jsou velmi drahé, takže optimalizace složení pufru a jeho pH metodou pokus-omyl je nákladná a neefektivní; vhodný model by umožnil odhadnout optimální podmínky, aby se protein nevysrážel.
Košovan zároveň popisuje, že smyslem modelování je posouvat základní porozumění směrem k aplikacím – například u elektroadheze, kde nízké napětí umožní „zapínat a vypínat“ adhezi mezi hydrogely či hydrogelem a tkání. Elektroadheze má slibné využití například v chirurgii, ale zatím chybí znalost jejího mechanismu, bez které jsme zase odkázáni na metodu pokus-omyl. Pochopení mechanismu elektroadheze je dalším z projektů, které Peter Košovan se svým týmem řeší v nově vzniklé výzkumné skupině MakroMolekulárního Modelování (MaMoMo).